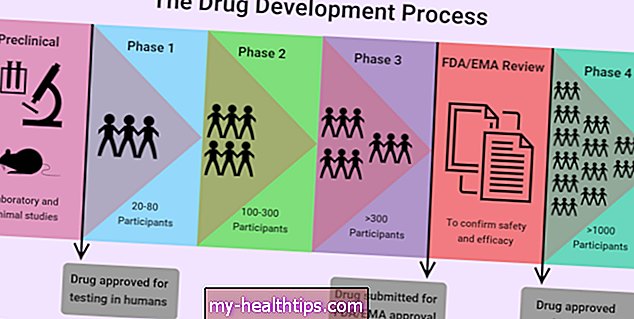
Клинические испытания проводятся по плану, известному как протокол. Протокол тщательно разработан, чтобы сбалансировать потенциальные преимущества и риски для участников, а также ответить на конкретные вопросы исследования. Протокол описывает следующее:
- цель исследования
- кто имеет право участвовать в испытании
- защита от рисков для участников
- подробности об исследованиях, процедурах и лечении
- как долго, как ожидается, продлится испытание
- какая информация будет собрана
Клиническое испытание проводится под руководством главного исследователя. Члены исследовательской группы регулярно следят за здоровьем участников, чтобы определить безопасность и эффективность исследования.
Воспроизведено с разрешения NIH Clinical Trials and You. NIH не поддерживает и не рекомендует какие-либо продукты, услуги или информацию, описанные или предлагаемые здесь Healthline. Последняя проверка страницы состоялась 20 октября 2017 г.
.jpg)